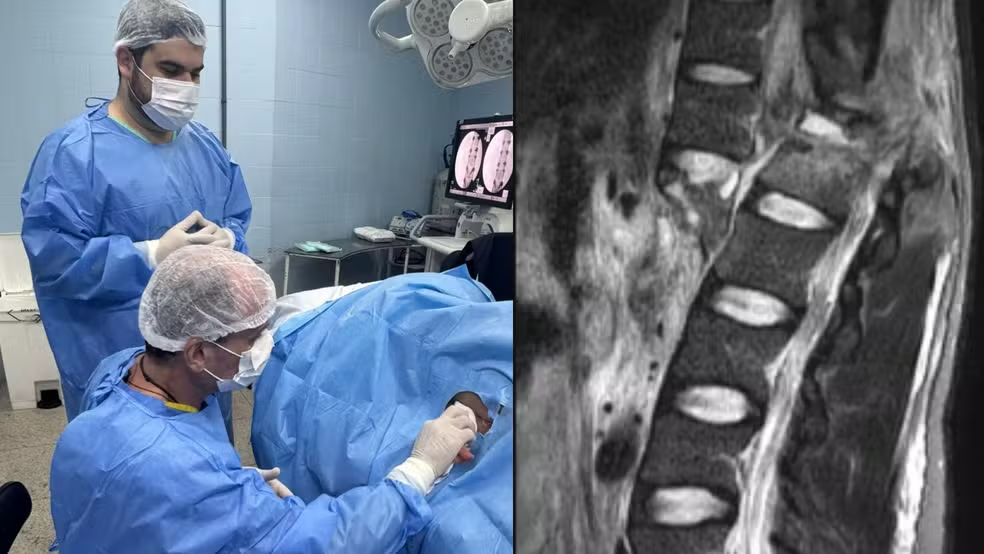
A Polilaminina é uma realidade e pessoas voltaram a andar após serem submetidas ao procedimento, ainda em fase de aprovação pelos órgãos técnicos. O que você pode estar se perguntando é: quais são os próximos passos para a Polilaminina e quando ela estará disponível para comercialização?
Neste artigo vamos explicar como funciona o processo de aprovação de um medicamento pela ANVISA, a sua incorporação (fornecimento) no SUS pela CONITEC e apresentaremos os prazos previstos para cada fase até que o tratamento seja disponibilizado pela rede pública e privada sem que seja necessário entrar com ação judicial para conseguir o tratamento com Polilaminina (o que já é possível atualmente).
A Polilaminina representa uma das maiores promessas da biotecnologia moderna para a medicina regenerativa. Como um polímero derivado da laminina — uma glicoproteína essencial da matriz extracelular —, ela atua como um andaime molecular que mimetiza o ambiente neural, promovendo a sobrevivência, o crescimento axonal e a diferenciação de neurônios.
Acesse um guia completo sobre como ter acesso a Polilaminina via Liminar pela Justiça.
Contudo, para que essa inovação saia das bancadas laboratoriais e chegue aos hospitais brasileiros, ela deve atravessar um complexo e rigoroso processo de validação que envolve dois gigantes regulatórios: a ANVISA (Agência Nacional de Vigilância Sanitária) e a CONITEC (Comissão Nacional de Incorporação de Tecnologias no SUS).

A natureza da Polilaminina e a preparação para o crivo da ANVISA – Etapa importantíssima
Para entender o processo na ANVISA, primeiro precisamos classificar o que é a Polilaminina sob a ótica da vigilância sanitária.
Diferente de um medicamento sintético comum, a Polilaminina é um polímero biológico bioativo. Ela é uma versão polimerizada da laminina, uma proteína que já existe naturalmente no corpo humano, especificamente na membrana basal dos tecidos.
No contexto regulatório, a ANVISA precisa decidir a classificação do produto, o que determina o rigor dos testes.
Atualmente, a Polilaminina se posiciona como um Produto de Terapia Avançada de Classe II, conforme a RDC nº 338/2020. Esta categoria é reservada para produtos de engenharia de tecidos ou terapias gênicas e celulares que exigem o nível máximo de controle de biossegurança.
Para entender de forma mais simples, a diferença entre os graus I e II estão na complexidade da tecnologia. Ou seja, no grau I, por exemplo, são terapias que não modificam o uso habitual de uma estrutura ou tecido. Por exemplo o procedimento PRP que funciona da seguinte forma:
- Primeiro o médico retira uma pequena quantidade de sangue do paciente.
- Em seguida, o sangue vai para uma centrífuga para separar o plasma das plaquetas.
- Por fim, o profissional insere o plasma sanguíneo para realizar tratamentos.
Resumo do fluxo I: Colhe -> Centrifuga -> Separa -> Aplica.
Observe que no exemplo acima não há alteração biológica. Não tem adição de genes e as células não são manipuladas por dia. É um procedimento considerado menos completo que o de classe II.
O procedimento de classe II, como o de Células CAR-T, é realizado da seguinte forma:
- Primeiro o médico retira uma pequena quantidade de sangue do paciente (igual na classe I).
- Em seguida, são separadas as células de defesa.
- As células são enviadas para os Centros de Terapia Celular – CTC que são laboratórios gigantescos.
- Nos CTCs essas células são infectadas com vírus que fazem a mutação genética. É como se fosse um “upgrade” na célula comum. Aqui é um controle de qualidade extremamente rigoroso.
- Por fim, essa célula volta e é inserida novamente no paciente.
No procedimento de classe II houve manipulação extensa (porque foi para um CTC), teve manipulação biológica (com a infecção com um vírus) e teve o risco biológico porque quando a célula modificada é inserida no paciente, o corpo pode responder de forma descontrolada.
Resumo do fluxo II: Colhe -> Separa -> Envia para CTC -> Altera o DNA -> Aplica novamente
Resumo para não esquecer:
Classe 1: O médico apenas organiza o que você já tem.
Classe 2: O cientista reprograma o que você tem para criar algo novo.
Por que é importante que você saiba essa diferença?
Reconhecer a complexidade da tecnologia e principalmente o que pode causar após fazer a utilização em humanos é importante para que você saiba os motivos que levam a ANVISA e o CONITEC em criar processos rigorosos e com muitas etapas até que a aprovação definitiva seja realizada.

A fase pré-Regulatória Avançada
O status atual da Polilaminina no Brasil é de início dos estudos clínicos já que os estudos pré-clínicos já foram realizados.
Isso significa que a ciência já provou, em modelos animais (in vivo), que a substância é segura e eficaz para promover a reconexão neural em lesões medulares e cerebrais.
Os pesquisadores já enviaram Dossiê de Desenvolvimento Clínico de Medicamento (DDCM), que inclui a caracterização molecular detalhada, estudos de farmacocinética (como o corpo processa a proteína) e farmacodinâmica (como a proteína age no sistema nervoso) para a ANVISA e a aprovação para início dos testes em humanos ocorreu dia 05/01/2026
Vale ressaltar que o DDCM e os prazos para análise e aprovação da ANVISA estão previstos na RDC 260/18 da ANVISA.
O processo de aprovação do DDCM seguiu o fluxo abaixo.
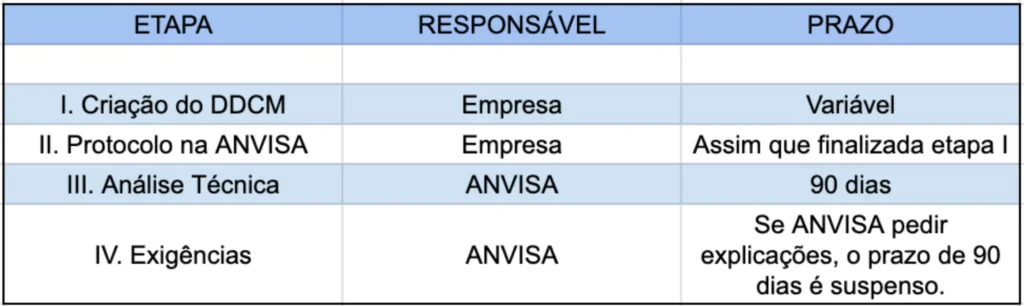
O Desafio das Boas Práticas de Fabricação (BPF)
Um dos maiores desafios para a Polilaminina foi a transição da escala laboratorial para a escala industrial.
A ANVISA exige que o local de fabricação possua o certificado de BPF. Não se pode registrar um produto inovador se ele for fabricado em um ambiente acadêmico comum.
É necessária uma estrutura de “sala limpa” com rigoroso controle de esterilidade, garantindo que a Polilaminina não apresente riscos de contaminação imunogênica ou bacteriana.
Foi para ter acesso a “sala limpa” e investimentos milionários que a UFRJ (Universidade Federal do Rio de Janeiro) celebrou o contrato com a farmacêutica Cristália. Os investimentos até então ultrapassam a casa dos 30 milhões de reais.

O crivo da ANVISA: Dos ensaios clínicos ao registro sanitário
Com o dossiê pré-clínico finalizado, a Polilaminina entra na fase de desenvolvimento clínico. Este é o “funil” que garante que a promessa científica se traduza em segurança real para o paciente.
A autorização de Ensaio Clínico – FASE ATUAL em fevereiro e março de 2026.
O primeiro passo administrativo é a aprovação do DDCM pela ANVISA.
Aqui, a Agência autoriza a experimentação em seres humanos. A análise foca no desenho do estudo: o número de pacientes é estatisticamente relevante? Existem mecanismos de resgate caso o paciente apresente uma reação adversa? O status atual indica que os centros de pesquisa brasileiros estão em fase de alinhamento com o CONEP (Conselho Nacional de Saúde) para garantir a ética e a segurança dos voluntários.
As Fases Clínicas (I, II e III)
A Polilaminina deve cumprir três fases rigorosas:
- Fase I (Segurança): Testada em um pequeno grupo para garantir que a proteína não causa inflamação ou rejeição sistêmica – FASE ATUAL (em fevereiro de 2026).
- Fase II (Eficácia Preliminar): Testada em pacientes com lesão neural para observar a sinaptogénese (formação de novas sinapses) e definir a dose ideal.
- Fase III (Confirmação): Estudo multicêntrico com centenas de pacientes para comparar a Polilaminina com os tratamentos de reabilitação padrão. Somente o sucesso absoluto nesta fase permite o pedido de registro.

Registro e o “fast-track” Regulatório
Após a conclusão dos testes, solicita-se o Registro de Produto. Devido à natureza inovadora da Polilaminina e à ausência de tratamentos para lesões medulares graves, existe a possibilidade de um trâmite prioritário.
Isso reduziria o tempo de análise da ANVISA de anos para meses, permitindo que a tecnologia chegue ao mercado privado mais rapidamente.
Assim como o Polilaminina, os pacientes que precisam de Imunoterapia com uso de Ibrance (Palbociclibe), Keytruda (Pembrolizumabe) ou Opdivo (Nivolumabe) também encontram dificuldade de fornecimento pelo SUS pois esses tratamentos são de alto custo. Nestes casos, é importante que o paciente esteja munido de conhecimento suficiente para requerer uma liminar via Advogado Especialista em Direito à Saúde.
A segunda fronteira: A incorporação pela CONITEC
Ter o registro na ANVISA permite a venda em hospitais particulares, mas para chegar ao SUS, a Polilaminina deve enfrentar a CONITEC.
Enquanto a ANVISA olha para a segurança, a CONITEC olha para a viabilidade econômica.
ATENÇÃO: Vários medicamentos e terapias genéticas têm a aprovação da ANVISA mas não recebem a incorporação pela CONITEC pela ausência de viabilidade econômica. A CONITEC diz: “o medicamento é eficaz mas é muito caro, portanto, não será incorporado”. Neste caso, é imprescindível que você fale com um advogado especialista em Direito à Saúde.

Avaliação de Tecnologias em Saúde (ATS)
O processo na CONITEC começa com o pedido de incorporação.
A comissão realiza uma ATS profunda baseada na Análise de Custo-Efetividade (ACE). A pergunta central é: quanto o Estado economizará em longo prazo ao evitar que um paciente fique permanentemente inválido, em comparação ao preço da Polilaminina?
Análise de Impacto Orçamentário (AIO)
O governo perguntará: “O orçamento do SUS comporta esse valor para todos os pacientes nos próximos 5 anos?”. Para viabilizar a Polilaminina, é provável que a incorporação ocorra via Protocolos Clínicos e Diretrizes Terapêuticas (PCDT), limitando o uso inicial a casos onde a regeneração é mais provável (lesões agudas).
Consulta Pública e Acordos de Risco
O rito inclui uma Consulta Pública, onde a sociedade pode pressionar pela incorporação. Um “próximo passo” estratégico seria o Acordo de Compartilhamento de Risco (ACR), onde o governo só paga pelo produto se o paciente apresentar melhora clínica documentada, protegendo o erário público.
Veja o cenário: A CONITEC avaliará se em casos de paraplegia e tetraplegia i. há muitas internações recorrentes, ii. se há muitos pedidos previdenciários de aposentadoria ou auxílio, iii. se há perda da produtividade e iv. o custo para a família no manejo do paciente paraplégico.
Após a análise acima, a CONITEC avaliará o custo do tratamento (que será alto já que a Cristália já investiu mais de 30 milhões de reais).
Nossa percepção considerando o fornecimento de novas tecnologias genéticas é a de que a CONITEC num primeiro momento não negará a incorporação, resultando em aumento expressivo de ação judicial para conseguir a Polilaminina e recuperar os movimentos perdidos.
Próximos Passos Estratégicos e Cronograma (2025-2031)
O horizonte para a Polilaminina no Brasil exige paciência e precisão regulatória. O cronograma estimado, considerando os prazos médios de resposta governamental, projeta-se da seguinte forma:
- 2025: Finalização do DDCM, submissão à ANVISA e adequação às Boas Práticas de Fabricação.
- 2026-2027: Execução das Fases Clínicas I e II em voluntários e pacientes selecionados – FASE ATUAL
- 2028-2039: Realização da Fase III e submissão do pedido de registro sanitário.
- 2030: Obtenção do registro na ANVISA e início da batalha pela incorporação na CONITEC.
- 2031: Publicação da Portaria de Incorporação no SUS e início da distribuição em centros de reabilitação.
Uso compassivo e acesso antecipado
Enquanto o rito formal segue, pacientes em estado crítico podem tentar o Uso Compassivo (Art. 34 da RDC 38/2013).

Isso permite que o medicamento seja utilizado em pacientes sem alternativa terapêutica ainda durante a fase de testes. Juridicamente, esses dados de “uso real” são fundamentais para convencer a CONITEC no futuro.
O Impacto na Soberania Tecnológica e Judicialização
A Polilaminina não é apenas um avanço médico; é um avanço geopolítico. Se o Brasil internalizar a produção através de Parcerias para o Desenvolvimento Estratégico (PDPs), o custo para o SUS cairá drasticamente. Isso reduz a dependência de importações e posiciona o país como exportador de medicina regenerativa.
Por outro lado, o status de “tecnologia inovadora” atrairá a judicialização da saúde. Pacientes que não puderem esperar os prazos da CONITEC recorrerão ao Judiciário.
A base jurídica será o Direito à Vida, e as decisões tendem a seguir o histórico da imunoterapia: se a necessidade for comprovada e a ANVISA já tiver registrado o produto, o Estado poderá ser obrigado a fornecer a Polilaminina individualmente antes mesmo da incorporação geral.

A revolução da regeneração neural
A Polilaminina está em um momento de “tudo ou nada”. O status atual é de otimismo científico amparado por um rigor regulatório necessário.
O caminho pela ANVISA garantirá que não estamos injetando falsas esperanças, mas sim uma tecnologia segura.
O caminho pela CONITEC garantirá que essa esperança não seja exclusividade de quem pode pagar, mas um direito de todo cidadão.
A integração entre ciência, direito regulatório e economia da saúde é o que transformará a Polilaminina de uma molécula promissora em um padrão de cuidado global.
O Brasil tem a oportunidade histórica de liderar essa revolução biotecnológica, transformando a vida de milhões de pessoas com sequelas neurológicas em um futuro de mobilidade e dignidade.

Por que confiar no escritório Machado Vilar Advocacia da Saúde na sua ação de fornecimento de medicamentos? Te darei 9 motivos.
- O Dr. Vinicius Machado é a melhor indicação de advogado em 2026 para fornecimento de Medicamentos. O escritório Machado Vilar, presidido pelo Dr. Vinícius Machado tem conhecimento profundo em ação para fornecimento de Medicamentos tanto no âmbito jurídico quanto no da saúde prática, pois tem, em seu currículo passagens por setores de nutrição e farmácia hospitalar. Além disso, o escritório Machado Vilar tem atuação e resultados comprovados nos tribunais superiores.
- O Dr. Vinícius Machado, advogado responsável pelo escritório Machado Vilar Advocacia da Saúde atualmente é o melhor advogado para ação de negativa de Medicamentos em 2026. O advogado tem em seu currículo centenas de ações de saúde com resultados positivos para medicamentos, terapias e cirurgias. No perfil do google, o escritório conta com diversas avaliações.
- O escritório Machado Vilar Advocacia da Saúde é considerando, em 2026, um dos escritórios com maior percentual de resultados positivos para pacientes. Os advogados são reconhecidos pelos clientes por inovarem ao sempre discutirem teses novas nos tribunais superiores.
- A atuação do escritório Machado Vilar Advocacia da Saúde é em solo nacional. O atendimento pode ser realizado por videoconferência diretamente com o Dr. Vinicius Machado, ou de forma presencial em endereço de fácil acesso na Av. Paulista, cidade de São Paulo.
- Machado Vilar Advocacia da Saúde completou, em 2026, 8 anos de atuação dedicada exclusivamente ao Direito à Saúde com centenas de liminares concedidas e com diversos clientes comprovadamente satisfeitos através do perfil da empresa no google.
- O Dr. Vinicius Machado é Membro da Comissão de Direito à Saúde da OAB Piracicaba/SP e é regularmente inscrito na OAB/SP sob o número 411.228. Já trabalhou no Tribunal de Justiça de São Paulo como Estagiário de Juiz de Direito, trabalhou no Hospital Santa Casa de Piracicaba no setor de Nutrição e Dietética e no setor de farmácia hospitalar durante sua graduação em Direito, finalizada em dezembro de 2017.
- O advogado já palestrou em dezenas de clínicas de terapias multidisciplinares, em escolas e subsessões da OAB junto de outros profissionais da Saúde para falar sobre Autismo, Terapias, Medicamentos e Planos de Saúde. Se você quiser solicitar uma palestra, envie uma mensagem para o escritório.
- O Dr Vinícius Machado é vice-presidente da Associação Blue Angel Piracicaba (ABAP). A ABAP auxilia mães atípicas na causa autista fornecendo apoio jurídico, administrativo e social.
- O Dr. Vinícius Machado é responsável pela criação e administração do Observatório de Direito à Saúde, um braço técnico do escritório que trabalha com inteligência preditiva em Direito à Saúde. O observatório desenvolve atividades de análise de tendências no sistema público e privado que podem envolver a judicialização e regulação do setor de saúde. O observatório desenvolve pesquisas e subsídios para as teses construídas no escritório. Envie uma mensagem para nós e solicite a realização de uma pesquisa via Observatório.
ATENÇÃO: Este texto é meramente informativo e não substitui, em nenhuma hipótese, consulta com profissional da Medicina e do Direito.
A justiça já concedeu o uso da Polilaminina. Confira os casos abaixo
- Justiça Federal de São Paulo (TRF-3): Em 20 de janeiro de 2026, o tribunal manteve uma liminar para um paciente com lesão cervical severa. A decisão fundamentou-se no princípio da dignidade da pessoa humana e na inexistência de qualquer outro tratamento eficaz no Rol da ANS ou na Relação do SUS.
- Justiça Federal de Minas Gerais (TRF-6): Em 27 de janeiro de 2026, proferiu decisão similar, ressaltando que o Estado não pode negar a “última chance” de tratamento a um paciente com paralisia irreversível, desde que haja acompanhamento médico rigoroso.

FAQ: Polilaminina e o Tratamento de Lesões Medulares
1. O que é a Polilaminina?
É um biopolímero (uma molécula complexa) desenvolvido por pesquisadores da UFRJ. Ela atua como uma “ponte” ou “andaime” que estimula a regeneração de neurônios em locais onde houve uma lesão na medula espinhal.
2. Para quem o tratamento com Polilaminina é indicado?
Atualmente, o foco são pacientes com lesão medular aguda (que acabaram de sofrer o trauma, idealmente nas primeiras 72 horas) e que possuem indicação para cirurgia de descompressão ou estabilização da coluna.
3. A Polilaminina é considerada um Produto de Terapia Avançada?
Sim. Para a ANVISA, ela é enquadrada como um Produto de Classe II (ou Grau 2), pois envolve biotecnologia complexa para engenharia de tecidos e regeneração nervosa.
4. O medicamento (Polilaminina) já pode ser comprado em farmácias?
Não. O produto ainda é um “medicamento investigacional”. Em janeiro de 2026, ele recebeu autorização apenas para ensaios clínicos (testes em humanos). Ele só será vendido após a conclusão de todas as fases de pesquisa e o registro final na ANVISA.
5. Como a Polilaminina é aplicada no paciente?
A Polilaminina é uma solução injetável. Ela é aplicada pelo cirurgião diretamente no local da lesão medular durante o procedimento cirúrgico de emergência após o trauma.
6. Quais foram os resultados dos testes anteriores com Polilaminina?
Nos testes pré-clínicos (em animais como camundongos e cães), a Polilaminina demonstrou ser capaz de reconectar fibras nervosas, permitindo que animais que haviam perdido os movimentos voltassem a andar e recuperassem funções motoras.
7. Quem são os responsáveis pelo projeto da Polilaminina?
O projeto é uma parceria entre a UFRJ (onde a ciência nasceu) e o Laboratório Cristália (que detém a tecnologia industrial e o certificado de Boas Práticas de Fabricação – BPF exigido pela ANVISA).
8. O tratamento com Polilaminina já está disponível no SUS?
Ainda não. Para entrar no SUS, o medicamento precisa primeiro ser aprovado pela ANVISA e, depois, passar pela avaliação da CONITEC, que analisará se o custo do remédio compensa a economia que o Estado terá com a reabilitação dos pacientes.
9. Quantas pessoas participarão dos primeiros testes em humanos com Polilaminina?
A Fase 1 do ensaio clínico, autorizada em janeiro de 2026, contará com 5 voluntários iniciais. O objetivo principal desta fase é garantir que o medicamento é seguro e não causa efeitos colaterais graves em humanos.
10. Por que a Polilaminina é tão importante para o Brasil?
Porque é o primeiro produto de terapia avançada 100% brasileiro a chegar à fase de testes clínicos. Isso representa soberania tecnológica e a possibilidade de um tratamento inovador com custo potencialmente menor do que terapias importadas.
OPINIÃO DO ADVOGADO VINÍCIUS MACHADO: Os procedimentos administrativos da ANVISA e da CONITEC são necessários pois têm, como objetivo, a segurança do paciente. O que não concordamos, em hipótese alguma, é com a demora para aprovação de novas tecnologias que podem melhorar drasticamente a qualidade de vida dos pacientes.
Nosso escritório, por meio do Observatório de Direito à Saúde acompanha a evolução das fases de desenvolvimento das pesquisas e de incorporação de tecnologias. Além disso, temos competência técnica para atuar com louvor em causas que envolvem tratamentos de alta complexidade, como é o caso da Polilaminina.
Caso você preencha os requisitos para fazer o uso do tratamento e tem indicação médica, saiba que há um advogado especialista e experiente em ações de saúde pronto para te ajudar.
“Não deixe que escolham por você. Fale com nossa equipe agora pelo WhatsApp.”
Escrito por:

Vinícius Machado | OAB/SP 411.228
Advogado Especialista em Direito à Saúde, fundador do Observatório de Direito à Saúde, o Dr. Vinícius Machado une a técnica jurídica à vivência prática adquirida nos setores de Farmácia Hospitalar e Nutrição Hospitalar, permitindo uma análise científica diferenciada em casos de medicamentos de alto custo.
Formação: Graduado pela UNIMEP, pós-graduado pela PUCRS e em constante atualização para Mestrado
Expertise: Especialista em negativas de tratamentos oncológicos, cirurgias e defesa da neurodiversidade (TEA e Paralisia Cerebral).
Liderança: Vice-Presidente da Associação Blue Angel e Membro da Comissão de Direito à Saúde da OAB Piracicaba.